HIDROCARBURI NESATURAȚI SAU NESATURI DIN SERIA ETILENEI
(ALCHENE SAU OLEFINE)
Alchenele, sau olefine(din latină olefiant - ulei - un nume vechi, dar folosit pe scară largă în literatura chimică. Motivul acestui nume a fost Clorura de etilenă, obținută în secolul al XVIII-lea, este o substanță lichidă, uleioasă.) - hidrocarburi alifatice nesaturate, în moleculele cărora există o legătură dublă între atomii de carbon.
Alchenele conțin mai puțini atomi de hidrogen în molecula lor decât alcanii corespunzători (cu același număr de atomi de carbon), prin urmare astfel de hidrocarburi sunt numite nelimitat sau nesaturat.
Alchenele formează o serie omoloagă cu formula generala CnH2n
1. Serii omoloage de alchene
|
CU nH2n alchenă |
Nume, sufix EH, ILENE |
|
C2H4 |
acest ro, acest Ilen |
|
C3H6 |
propenă |
|
C4H8 |
butenă |
|
C5H10 |
penten |
|
C6H12 |
hexenă |
Omologi:
CUH 2 = CH 2 etena
CUH 2 = CH- CH 3 propenă
CUH2=CH-CH2-CH3butenă-1
CUH2 =CH-CH2-CH2-CH 3 penten-1
2. Proprietăți fizice
Etilena (etena) este un gaz incolor cu un miros dulceag foarte slab, puțin mai ușor decât aerul, ușor solubil în apă.
C 2 – C 4 (gaze)
C 5 – C 17 (lichide)
C 18 – (solid)
· Alchenele sunt insolubile în apă, solubile în solvenți organici (benzină, benzen etc.)
Mai ușor decât apa
Odată cu creșterea Mr, punctele de topire și de fierbere cresc
3. Cea mai simplă alchenă este etilena - C2H4
Formulele structurale și electronice ale etilenei sunt:
În molecula de etilenă se suferă hibridizare s- si doi p-orbitalii atomilor de C ( sp 2 -hibridare).
Astfel, fiecare atom de C are trei orbitali hibrizi și unul nehibrid p-orbitali. Doi dintre orbitalii hibrizi ai atomilor de C se suprapun reciproc și se formează între atomii de C
σ - legătură. Cei patru orbiti hibrizi rămași ai atomilor de C se suprapun în același plan cu patru s-orbitali ai atomilor de H și formează, de asemenea, patru legături σ -. Două non-hibride p-orbitalii atomilor de C se suprapun reciproc intr-un plan care este situat perpendicular pe planul legaturii σ, i.e. se formează unul P- conexiune.

Prin natura ei P- conexiunea este net diferită de σ - conexiune; P- legatura este mai putin puternica datorita suprapunerii norilor de electroni in afara planului moleculei. Sub influența reactivilor P- conexiunea se rupe usor.
Molecula de etilenă este simetrică; nucleele tuturor atomilor sunt situate în același plan și unghiurile de legătură sunt apropiate de 120°; distanța dintre centrele atomilor de C este de 0,134 nm.
Dacă atomii sunt legați printr-o legătură dublă, atunci rotația lor este imposibilă fără nori de electroni P- conexiunea nu a fost deschisă.
4. Izomeria alchenelor
Împreună cu izomeria structurală a scheletului de carbon Alchenele sunt caracterizate, în primul rând, de alte tipuri de izomerie structurală - izomerie de poziție a legăturilor multipleȘi izomerie interclasă.
În al doilea rând, în seria alchenelor există izomerie spațială , asociate cu diferite poziții ale substituenților față de legătura dublă, în jurul căreia rotația intramoleculară este imposibilă.
Izomeria structurală a alchenelor
1. Izomeria scheletului de carbon (începând de la C 4 H 8):
2. Izomeria poziției dublei legături (începând de la C 4 H 8):
3. Izomerie interclasică cu cicloalcani, începând cu C 3 H 6:
Izomeria spațială a alchenelor
Rotația atomilor în jurul unei duble legături este imposibilă fără a o rupe. Acest lucru se datorează caracteristicilor structurale ale legăturii p (norul de electroni p este concentrat deasupra și sub planul moleculei). Datorită fixării rigide a atomilor nu apare izomeria rotațională față de legătura dublă. Dar devine posibil cis-transă-izomerie.
Alchenele, care au substituenți diferiți pe fiecare dintre cei doi atomi de carbon de la legătura dublă, pot exista sub forma a doi izomeri spațiali, diferiți prin localizarea substituenților față de planul legăturii p. Deci, în molecula butenă-2 CH3 –CH=CH–CH3 Grupările CH3 pot fi localizate fie pe o parte a dublei legături în cis-izomer, sau pe laturile opuse in transă-izomer.

ATENŢIE!
cis-trans- Izomeria nu apare dacă cel puțin unul dintre atomii de C de la legătura dublă are 2 substituenți identici.
De exemplu,
butenă-1 CH 2 = CH – CH 2 – CH 3 nu are cis- Și transă-izomeri, deoarece Primul atom de C este legat de doi atomi de H identici.
Izomeri cis- Și transă- diferă nu numai fizic
 ,
,
dar şi proprietăţi chimice, deoarece aducerea unor părți ale unei molecule mai aproape sau mai departe unele de altele în spațiu promovează sau împiedică interacțiunea chimică.
Uneori cis-trans-izomeria nu se numește destul de exact izomerie geometrică. Inexactitatea este că Toate izomerii spațiali diferă prin geometria lor și nu numai cis- Și transă-.
5. Nomenclatură
Alchenele cu structură simplă sunt adesea denumite prin înlocuirea sufixului -ane în alcani cu -ilenă: etan - etilenă, propan - propilenă etc.
Conform nomenclaturii sistematice, denumirile hidrocarburilor de etilenă se realizează prin înlocuirea sufixului -ane din alcanii corespunzători cu sufixul -enă (alcan - alchenă, etan - etenă, propan - propenă etc.). Alegerea lanțului principal și ordinea denumirii sunt aceleași ca pentru alcani. Cu toate acestea, lanțul trebuie să includă în mod necesar o legătură dublă. Numerotarea lanțului începe de la capătul de care se află cel mai apropiat această legătură. De exemplu:

Radicalii nesaturați (alchene) sunt numiți prin nume banale sau prin nomenclatură sistematică:
(H2C=CH-)vinil sau etenil
(H2C=CH-CH2) alil
Conținând o legătură pi sunt hidrocarburile nesaturate. Sunt derivați ai alcanilor, în moleculele cărora au fost eliminați doi atomi de hidrogen. Se formează valențele libere rezultate tip nou legătură care este perpendiculară pe planul moleculei. Așa apare un grup nou compuși – alchene. Vom lua în considerare proprietățile fizice, producția și utilizarea substanțelor din această clasă în viața de zi cu zi și în industrie în acest articol.
Serii omoloage de etilenă
Formula generală a tuturor compușilor numiți alchene, reflectând compoziția lor calitativă și cantitativă, este C n H 2 n. Denumirile hidrocarburilor conform nomenclaturii sistematice au următoarea formă: în termenul alcanului corespunzător sufixul se schimbă din -an în -enă, de exemplu: etan - etenă, propan - propenă etc. În unele surse găsiți un alt nume pentru compușii din această clasă - olefine. În continuare vom studia procesul de formare a dublei legături și proprietăți fizice alchene și, de asemenea, determină dependența lor de structura moleculei.
Cum se formează o legătură dublă?
Folosind exemplul etilenei, natura electronică a legăturii pi poate fi reprezentată astfel: atomii de carbon din molecula sa sunt sub formă de hibridizare sp 2. În acest caz, se formează o legătură sigma. Încă doi orbitali hibrizi, câte unul din atomi de carbon, formează legături sigma simple cu atomii de hidrogen. Cei doi nori hibrizi liberi rămași de atomi de carbon se suprapun deasupra și sub planul moleculei - se formează o legătură pi. Acesta este cel care determină proprietățile fizice și chimice ale alchenelor, care vor fi discutate în continuare.

Izomerie spațială
Compuși având același cantitativ și compoziție de înaltă calitate moleculele, dar diferite structuri spațiale, se numesc izomeri. Izomeria apare într-un grup de substanțe numite organice. Caracteristicile olefinelor sunt mult influențate de fenomenul de izomerie optică. Se exprimă prin faptul că omologii etilenei, care conțin diferiți radicali sau substituenți la fiecare dintre cei doi atomi de carbon de la legătura dublă, pot apărea sub forma a doi izomeri optici. Ele diferă unele de altele prin poziția substituenților în spațiu față de planul dublei legături. Proprietățile fizice ale alchenelor în acest caz vor fi, de asemenea, diferite. De exemplu, aceasta se referă la punctele de fierbere și de topire ale substanțelor. Astfel, olefinele cu un schelet de carbon drept au puncte de fierbere mai mari decât compușii izomeri. De asemenea, punctele de fierbere ale izomerilor cis ai alchenelor sunt mai mari decât ale izomerilor trans. În ceea ce privește temperaturile de topire, imaginea este inversă.
Caracteristici comparative ale proprietăților fizice ale etilenei și omologilor săi
Primii trei reprezentanți ai olefinelor sunt compuși gazoși, apoi, începând cu pentenă C 5 H 10 și terminând cu o alchenă cu formula C 17 H 34, sunt lichide și apoi există solide. La omologii etenei se poate observa următoarea tendință: punctele de fierbere ale compușilor scad. De exemplu, pentru etilenă acest indicator este -169,1 °C, iar pentru propilenă -187,6 °C. Dar temperaturile de fierbere cresc odată cu creșterea greutății moleculare. Deci, pentru etilenă este -103,7°C, iar pentru propenă -47,7°C. Pentru a rezuma ceea ce s-a spus, putem trage o scurtă concluzie: proprietățile fizice ale alchenelor depind de greutatea moleculară a acestora. Pe măsură ce crește, se schimbă starea de agregare compuși în direcția: gaz - lichid - solid, iar punctul de topire scade, iar punctul de fierbere crește.

Caracteristicile etenei
Primul reprezentant serie omoloagă alchenele sunt etilena. Este un gaz, ușor solubil în apă, dar foarte solubil în solvenți organici și nu are culoare. Greutate moleculară - 28, etena este puțin mai ușoară decât aerul, are un miros dulce și dulce. Reacționează ușor cu halogeni, hidrogen și halogenuri de hidrogen. Proprietățile fizice ale alchenelor și parafinelor sunt totuși destul de asemănătoare. De exemplu, starea de agregare, capacitatea metanului și etilenei de a suferi o oxidare severă etc. Cum se pot distinge alchenele? Cum se identifică natura nesaturată a unei olefine? În acest scop, există reacții calitative, asupra cărora ne vom opri mai detaliat. Să ne amintim ce particularitate au alchenele în structura moleculei. Proprietățile fizice și chimice ale acestor substanțe sunt determinate de prezența unei duble legături în compoziția lor. Pentru a-i dovedi prezența, treceți hidrocarbura gazoasă printr-o soluție violetă de permanganat de potasiu sau apă cu brom. Dacă devin decolorate, înseamnă că compusul conține legături pi în moleculele sale. Etilena intră într-o reacție de oxidare și decolorează soluțiile de KMnO4 și Br2.
Mecanismul reacțiilor de adiție
Scindarea dublei legături se termină cu adăugarea altor atomi la valențele libere ale carbonului elemente chimice. De exemplu, atunci când etilena reacţionează cu hidrogenul, numită hidrogenare, produce etan. Este necesar un catalizator cum ar fi nichel sub formă de pulbere, paladiu sau platină. Reacția cu HCI se încheie cu formarea cloretanului. Alchenele care conțin mai mult de doi atomi de carbon în moleculele lor suferă adăugarea de halogenuri de hidrogen ținând cont de regula lui V. Markovnikov.

Cum interacționează omologii etenei cu halogenurile de hidrogen
Dacă ne confruntăm cu sarcina „Caracterizarea proprietăților fizice ale alchenelor și prepararea lor”, trebuie să luăm în considerare regula lui V. Markovnikov mai detaliat. S-a stabilit în practică că omologii etilenei reacţionează cu clorura de hidrogen şi alţi compuşi la locul clivajului dublei legături, respectând un anumit model. Constă în faptul că un atom de hidrogen este atașat celui mai hidrogenat atom de carbon, iar un ion de clor, brom sau iod este atașat atomului de carbon care conține cel mai mic număr de atomi de hidrogen. Această caracteristică a apariției reacțiilor de adiție se numește regula lui V. Markovnikov.
Hidratarea și polimerizarea
Să continuăm să luăm în considerare proprietățile fizice și aplicațiile alchenelor folosind exemplul primului reprezentant al seriei omoloage - etena. Reacția sa cu apa este folosită în industria de sinteză organică și are un rol important semnificație practică. Procesul a fost efectuat pentru prima dată în secolul al XIX-lea de către A.M. Butlerov. Reacția necesită îndeplinirea unui număr de condiții. Aceasta este, în primul rând, utilizarea acidului sulfuric concentrat sau oleum ca catalizator și solvent etenic, o presiune de aproximativ 10 atm și o temperatură în 70°. Procesul de hidratare are loc în două faze. În primul rând, în locul în care legătura pi este ruptă, moleculele de acid sulfat se unesc cu etena, rezultând formarea acidului etil sulfuric. Substanța rezultată reacționează apoi cu apa pentru a obține etanol. Etanolul este un produs important utilizat în Industria alimentară pentru producția de materiale plastice, cauciucuri sintetice, lacuri și alte produse chimice organice.

Polimeri pe bază de olefine
Continuând să studiem problema utilizării substanțelor aparținând clasei alchenelor, vom studia procesul de polimerizare a acestora, la care pot participa compuși care conțin legături chimice nesaturate în compoziția moleculelor lor. Există mai multe tipuri de reacții de polimerizare care produc produse cu greutate moleculară mare - polimeri, cum ar fi polietilena, polipropilena, polistirenul etc. Mecanismul radicalilor liberi duce la producerea de polietilenă. presiune ridicata. Este unul dintre cei mai folosiți compuși în industrie. Tipul cation-ion asigură producerea unui polimer cu o structură stereoregulată, de exemplu polistiren. Este considerat unul dintre cei mai siguri și mai convenabil polimeri de utilizat. Produsele din polistiren sunt rezistente la substanțele agresive: acizi și alcalii, neinflamabile și ușor de vopsit. Un alt tip de mecanism de polimerizare este dimerizarea, care duce la producerea de izobutenă, care este folosită ca aditiv antidetonant pentru benzină.
Metode de obținere
Alchenele, ale căror proprietăți fizice le studiem, sunt obținute în laborator și în industrie diverse metode. În experimentele din cursul școlar de chimie organică, se utilizează procesul de deshidratare a alcoolului etilic cu ajutorul agenților de îndepărtare a apei, de exemplu, cum ar fi pentoxidul de fosfor sau acidul sulfat. Reacția are loc atunci când este încălzită și este proces invers obţinerea etanolului. O altă metodă comună de producere a alchenelor și-a găsit aplicația în industrie și anume: încălzirea derivaților halogenați ai hidrocarburilor saturate, de exemplu, clorpropanul cu soluții concentrate de alcool de alcalii - hidroxid de sodiu sau potasiu. În reacție, o moleculă de acid clorhidric este eliminată și se formează o dublă legătură în locul unde apar valențele libere ale atomilor de carbon. Produsul final al procesului chimic va fi o olefină - propenă. Continuând să luăm în considerare proprietățile fizice ale alchenelor, să ne oprim asupra principalului proces de producere a olefinelor - piroliza.

Producția industrială de hidrocarburi nesaturate din seria etilenei
Materii prime ieftine - gazele formate în timpul cracării petrolului, servesc ca sursă de olefine în industria chimica. În acest scop, se utilizează o schemă tehnologică de piroliză - scindarea unui amestec de gaze, care are loc odată cu ruperea legăturilor de carbon și formarea de etilenă, propenă și alte alchene. Piroliza se realizează în cuptoare speciale formate din bobine de piroliză individuale. Acestea creează o temperatură de aproximativ 750-1150°C și conțin vapori de apă ca diluant. Reacțiile au loc printr-un mecanism în lanț cu formarea de radicali intermediari. Produsul final este etilena sau propena, acestea sunt produse în volume mari.

Am studiat în detaliu proprietățile fizice, precum și aplicațiile și metodele de producere a alchenelor.
Alchenele se caracterizează în primul rând prin reacții aderare printr-o legătură dublă. Practic, aceste reacții au loc printr-un mecanism ionic. Legătura pi este ruptă și se formează două noi legături sigma. Permiteți-mi să vă reamintesc că reacțiile de substituție au fost tipice pentru alcani și au urmat un mecanism radical. Moleculele de hidrogen se pot atașa la alchene; aceste reacții se numesc hidrogenare, molecule de apă, hidratare, halogenare, halogenare, hidrohalogenare. Dar mai întâi lucrurile.
Reacții de adiție cu duble legătură
Asa de, primul proprietate chimică capacitatea de a adăuga halogenuri de hidrogen, hidrohalogenare.
Propena și alte alchene reacționează cu halogenurile de hidrogen conform regulii lui Markovnikov.

Un atom de hidrogen se atașează de cel mai hidrogenat, sau mai corect hidrogenat, atom de carbon.
Al doilea numărul de pe lista noastră de proprietăți ar fi hidratarea, adăugarea de apă.
Reacția are loc atunci când este încălzită în prezența unui acid, de obicei sulfuric sau fosforic. Adăugarea de apă are loc și în conformitate cu regula lui Markovnikov, adică alcoolul primar poate fi obținut numai prin hidratarea etilenei, restul alchenelor neramificate dau alcooli secundari.
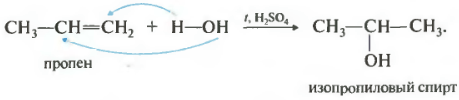
Există excepții de la regula lui Markovnikov atât pentru hidrohalogenare, cât și pentru hidratare. În primul rând, contrar acestei reguli, adăugarea are loc în prezența peroxizilor.
În al doilea rând, pentru derivații de alchene în care sunt prezente grupări atrăgătoare de electroni. De exemplu, pentru 3,3,3-trifluorpropen-1.

Atomii de fluor, datorită electronegativității lor ridicate, atrag densitatea de electroni către ei înșiși de-a lungul unui lanț de legături sigma. Acest fenomen se numește efect inductiv negativ.
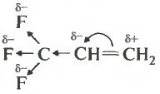
Din această cauză, electronii pi mobili ai dublei legături sunt deplasați și atomul de carbon cel mai exterior ajunge cu o sarcină pozitivă parțială, care este de obicei desemnată ca delta plus. De aici se va duce ionul de brom încărcat negativ, iar cationul de hidrogen se va atașa de atomul de carbon cel mai puțin hidrogenat.
În plus față de gruparea trifluormetil, de exemplu, gruparea triclorometil, gruparea nitro, gruparea carboxil și unele altele au un efect inductiv negativ.
Acest al doilea caz de încălcare a regulii Markovnikov în examenul de stat unificat este foarte rar, dar este totuși recomandabil să îl țineți cont dacă intenționați să promovați examenul cu punctajul maxim.
Al treilea Proprietatea chimică atașarea moleculelor de halogen.

Aceasta se referă în primul rând la brom, deoarece această reacție este calitativă pentru o legătură multiplă. Când se trece, de exemplu, etilena prin apă cu brom, adică o soluție de brom în apă având culoarea maro, se decolorează. Dacă treceți un amestec de gaze, de exemplu, etan și etenă, prin apă cu brom, puteți obține etan pur, fără impurități etene, deoarece va rămâne în balonul de reacție sub formă de dibrometan, care este un lichid.
De remarcată este reacția alchenelor în faza gazoasă cu încălzire puternică, de exemplu, cu clorul.
În astfel de condiții, nu are loc o reacție de adiție, ci o reacție de substituție. Mai mult, exclusiv la atomul de carbon alfa, adică atomul adiacent dublei legături. În acest caz, se obține 3-cloropropen-1. Aceste reacții sunt rare la examen, așa că majoritatea studenților nu le amintesc și, de regulă, greșesc.
Al patrulea numărul este reacția de hidrogenare și odată cu ea reacția de dehidrogenare. Adică adăugarea sau îndepărtarea hidrogenului.

Hidrogenarea are loc nu foarte temperatura ridicata pe un catalizator de nichel. La temperaturi mai ridicate, dehidrogenarea este posibilă pentru a produce alchine.
a cincea O proprietate a alchenelor este capacitatea de a polimeriza, atunci când sute și mii de molecule de alchenă formează lanțuri foarte lungi și puternice datorită ruperii legăturii pi și formării de legături sigma între ele.
În acest caz, rezultatul a fost polietilena. Vă rugăm să rețineți că molecula rezultată nu conține legături multiple. Astfel de substanțe sunt numite polimeri, moleculele originale sunt numite monomeri, fragmentul care se repetă este unitatea elementară a polimerului, iar numărul n este gradul de polimerizare.
Reacții producând alte importante materiale polimerice, de exemplu, polipropilenă.
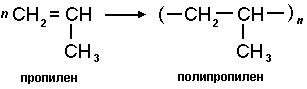
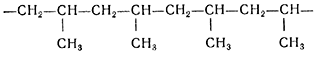
Un alt polimer important este clorura de polivinil.

Materialul de pornire pentru producerea acestui polimer este cloroetena, al cărei nume comun este clorură de vinil. Deoarece acest substituent nesaturat se numește vinil. O abreviere comună pe plastic Produse din PVC reprezintă doar clorură de polivinil.
Am discutat cinci proprietăți care au reprezentat reacții de adiție a legăturii duble. Acum să ne uităm la reacții oxidare.
Reacții de oxidare a alchenei
Şaselea Proprietatea chimică din lista noastră generală este oxidarea ușoară sau reacția Wagner. Apare atunci când o alchenă este expusă la o soluție apoasă de permanganat de potasiu la rece, motiv pentru care temperatura de zero grade este adesea indicată în sarcinile de examen.
Rezultatul este un alcool dihidroxilic. În acest caz, etilenglicolul, dar în general astfel de alcooli sunt denumirea comună glicoli În timpul reacției, soluția de permanganat violet-roz devine decolorată, deci această reacție este și calitativă pentru o legătură dublă. Manganul într-un mediu neutru este redus de la starea de oxidare +7 la starea de oxidare +4. Să ne uităm la câteva exemple suplimentare. ECUAȚIA
Aici obținem propandiol-1,2. Cu toate acestea, alchenele ciclice vor reacționa în același mod. ECUAȚIA
O altă opțiune este atunci când legătura dublă este situată, de exemplu, în lanțul lateral al hidrocarburilor aromatice. În mod regulat teme de examen Există o reacție Wagner care implică stiren, al doilea nume este vinilbenzen.

Sper că v-am oferit suficiente exemple pentru a înțelege că oxidarea ușoară a unei legături duble se supune întotdeauna destul de regula simpla Legătura pi este ruptă și se adaugă o grupare hidroxi la fiecare atom de carbon.
Acum, referitor la oxidarea dură. Va fi al nostru al șaptelea proprietate. Această oxidare are loc atunci când o alchenă reacţionează cu o soluţie acidă de permanganat de potasiu când este încălzită.
Are loc distrugerea moleculei, adică distrugerea ei la dubla legătură. În cazul butenului-2, s-au obținut două molecule de acid acetic. În general, poziția legăturii multiple în lanțul de carbon poate fi apreciată din produsele de oxidare.
Oxidarea butenei-1 produce o moleculă de acid propionic (propanoic) și dioxid de carbon.
În cazul etilenei, obțineți două molecule de dioxid de carbon. În toate cazurile, într-un mediu acid, manganul este redus din starea de oxidare +7 la +2.
Și, în sfârșit Al optulea proprietate oxidare completă sau ardere.
Alchenele ard, ca și alte hidrocarburi, până la dioxid de carbon și apă. Să scriem ecuația pentru arderea alchenelor în formă generală.
Vor exista tot atâtea molecule de dioxid de carbon câte atomi de carbon există în molecula de alchenă, deoarece molecula de CO 2 conține un atom de carbon. Adică n molecule de CO2. Vor fi de două ori mai puține molecule de apă decât atomii de hidrogen, adică 2n/2, ceea ce înseamnă doar n.
Există același număr de atomi de oxigen în stânga și în dreapta. În dreapta sunt 2n de dioxid de carbon plus n de apă, pentru un total de 3n. În stânga există același număr de atomi de oxigen, ceea ce înseamnă că sunt de două ori mai puține molecule, deoarece molecula conține doi atomi. Adică 3n/2 molecule de oxigen. Puteți scrie 1.5n.
Am revizuit opt proprietățile chimice ale alchenelor.
Să aflăm care este reacția de hidratare a alchenei. Pentru asta vom da descriere scurta această clasă de hidrocarburi.
Formula generala
Alchenele sunt compuși organici nesaturați cu formula generală SpH2n, ale căror molecule au o legătură dublă și conțin, de asemenea, legături simple (simple). Atomii de carbon sunt în stare hibrid sp2. Reprezentanții acestei clase sunt numiți etilenă, deoarece strămoșul acestei serii este etilena.
Caracteristicile nomenclaturii
Pentru a înțelege mecanismul hidratării alchenelor, este necesar să evidențiem trăsăturile denumirilor lor. Conform nomenclaturii sistematice, la denumirea unei alchene se folosește un anumit algoritm de acțiuni.
În primul rând, trebuie să determinați cel mai lung lanț de carbon care include o legătură dublă. Numerele indică locația radicalilor de hidrocarburi, începând cu cel mai mic din alfabetul rus.
Dacă există mai mulți radicali identici în moleculă, prefixele de calificare di-, tri- și tetra sunt adăugate la nume.
Abia după aceasta se denumește însuși lanțul de atomi de carbon, adăugând la sfârșit sufixul -ene. Pentru a clarifica locația unei legături nesaturate (duble) într-o moleculă, aceasta este indicată printr-un număr. De exemplu, 2metilpenten-2.

Hibridarea în alchene
Pentru a face față unei sarcini de următorul tip: „Stabiliți formula moleculară a unei alchene, a cărei hidratare a produs un alcool secundar”, este necesar să aflați caracteristicile structurale ale reprezentanților acestei clase de hidrocarburi. Prezența unei duble legături explică capacitatea CxHy de a intra în reacții de adiție. Unghiul dintre legăturile duble este de 120 de grade. Nu se observă rotație în legătura nesaturată, astfel încât reprezentanții acestei clase sunt caracterizați prin izomerie geometrică. Principalul loc de reacție în moleculele de alchenă este legătura dublă.

Proprietăți fizice
Sunt similare cu hidrocarburile saturate. Reprezentanții inferiori ai acestei clase de hidrocarburi organice sunt substanțele gazoase în condiții normale. În continuare, se observă o tranziție treptată la lichide, iar alchenele, ale căror molecule conțin mai mult de șaptesprezece atomi de carbon, se caracterizează printr-o stare solidă. Toți compușii din această clasă au o solubilitate nesemnificativă în apă, în timp ce sunt perfect solubili în solvenți organici polari.
Caracteristicile izomeriei
Prezența compușilor de etilenă în molecule explică diversitatea formulelor structurale ale acestora. În plus față de izomerizarea scheletului de carbon, care este caracteristică reprezentanților tuturor claselor de compuși organici, au izomeri interclase. Sunt cicloparafine. De exemplu, pentru propenă, izomerul interclaselor este ciclopropanul.
Prezența unei duble legături în moleculele din această clasă explică posibilitatea izomeriei geometrice cis și trans. Astfel de structuri sunt posibile numai pentru hidrocarburile nesaturate simetrice care conțin o legătură dublă.
Existența acestei variante de izomerie este determinată de imposibilitatea rotației libere a atomilor de carbon de-a lungul dublei legături.

Specificul proprietăților chimice
Mecanismul de hidratare al alchenelor are anumite caracteristici. Această reacție se referă la adiție electrofilă.
Cum decurge reacția de hidratare a unei alchene? Pentru a răspunde la această întrebare, luați în considerare regula lui Markovnikov. Esența sa este că hidratarea alchenelor cu structură asimetrică se realizează într-un anumit mod. Atomul de hidrogen se va atașa de carbonul care este mai hidrogenat. Gruparea hidroxil este atașată la un atom de carbon care are mai puțin H. Hidratarea alchenelor duce la formarea de alcooli monohidroxilici secundari.
Pentru ca reacția să se desfășoare pe deplin, acizii minerali sunt utilizați ca catalizatori. Acestea garantează introducerea în amestecul de reacție cantitatea necesară cationi de hidrogen.
Este imposibil să se obțină alcooli monohidric primari prin hidratarea alchenelor, deoarece regula lui Markovnikov nu va fi respectată. Această caracteristică utilizat în sinteza organică a alcoolilor secundari. Orice hidratare a alchenelor se realizează fără utilizarea condițiilor dure, astfel încât procesul și-a găsit utilizarea practică.
Dacă etilena este luată ca reprezentant inițial al clasei SpH2n, regula lui Markovnikov nu funcționează. Ce alcooli nu se pot obține prin hidratarea alchenelor? Este imposibil să se obțină alcooli primari din alchene nesimetrice ca urmare a unui astfel de proces chimic. Cum se utilizează hidratarea alchenelor? Producția de alcooli secundari se realizează exact în acest mod. Dacă un reprezentant al seriei de acetilenă (alchine) este ales ca hidrocarbură, hidratarea duce la producerea de cetone și aldehide.

Conform regulii lui Markovnikov, se realizează hidratarea alchenelor. Reacția are un mecanism de adiție electrofilă, a cărui esență este bine studiată.
Să dăm câteva exemple specifice de astfel de transformări. La ce duce hidratarea alchenelor? Exemplele oferite într-un curs de chimie școlar indică faptul că propanol-2 poate fi obținut din propenă prin reacția cu apă, iar butanol-2 poate fi obținut din buten-1.
Hidratarea cu alchene este utilizată comercial. În acest fel se obțin alcooli secundari.

Halogenare
Interacțiunea hidrocarburilor nesaturate cu moleculele de halogen este considerată o reacție calitativă la o legătură dublă. Am analizat deja cum are loc hidratarea alchenelor. Mecanismul de halogenare este similar.
Moleculele de halogen au o legătură chimică covalentă nepolară. Când apar fluctuații temporare, fiecare moleculă devine electrofilă. Ca urmare, probabilitatea de adăugare crește, însoțită de distrugerea dublei legături din moleculele de hidrocarburi nesaturate. După terminarea procesului, produsul de reacție este un derivat dihalogen al alcanului. Bromurarea este considerată o reacție calitativă la hidrocarburile nesaturate, deoarece culoarea maro a halogenului dispare treptat.

Hidrohalogenare
Ne-am uitat deja la care este formula pentru hidratarea alchenelor. Reacțiile cu bromură de hidrogen au o opțiune similară. Acest compus anorganic are o legătură chimică polară covalentă, deci există o schimbare a densității electronilor către atomul de brom mai electronegativ. Hidrogenul capătă o sarcină parțială pozitivă, dând un electron halogenului și atacă molecula de alchenă.
Dacă o hidrocarbură nesaturată are o structură asimetrică, atunci când reacţionează cu o halogenură de hidrogen, se formează doi produşi. Astfel, din propenă în timpul hidrohalogenării se obțin 1-bromoproan și 2-bromopropan.
Pentru evaluarea preliminară opțiunile de interacțiune țin cont de electronegativitatea substituentului selectat.
Oxidare
Legătura dublă inerentă moleculelor de hidrocarburi nesaturate este expusă agenților oxidanți puternici. De asemenea, sunt de natură electrofilă și sunt utilizate în industria chimică. Un interes deosebit este oxidarea alchenelor cu o soluție apoasă (sau slab alcalină) de permanganat de potasiu. Se numește reacție de hidroxilare deoarece are ca rezultat alcooli dihidroxilici.
De exemplu, atunci când moleculele de etilenă sunt oxidate cu o soluție apoasă de permanganat de potasiu, se obține etinediol-1,2 (etilen glicol). Această interacțiune este considerată o reacție calitativă la o legătură dublă, deoarece în timpul interacțiunii se observă decolorarea soluției de permanganat de potasiu.
Într-un mediu acid (în condiții dure), aldehida poate fi remarcată printre produșii de reacție.
Când interacționează cu oxigenul atmosferic, alchena corespunzătoare este oxidată la dioxid de carbon și vapori de apă. Procesul este însoțit de eliberarea de energie termică, astfel încât în industrie este folosit pentru a genera căldură.
Prezența unei duble legături într-o moleculă de alchenă indică posibilitatea ca reacții de hidrogenare să apară în această clasă. Interacțiunea SpH2n cu moleculele de hidrogen are loc atunci când platina și nichelul sunt utilizate termic ca catalizatori.
Mulți reprezentanți ai clasei de alchene sunt predispuși la ozonare. La temperaturi scăzute, reprezentanții acestei clase reacționează cu ozonul. Procesul este însoțit de scindarea dublei legături, formarea de compuși peroxidici ciclici numiți ozonide. Moleculele lor conțin Comunicații O-O, prin urmare substantele sunt explozive. Ozonidele nu sunt sintetizate în formă pură, ele sunt descompuse printr-un proces de hidroliză, apoi reduse cu zinc. Produșii acestei reacții sunt compuși carbonilici, care sunt izolați și identificați de cercetători.

Polimerizare
Această reacție implică combinarea secvențială a mai multor molecule de alchenă (monomeri) într-o macromoleculă mare (polimer). Din etena de pornire se obţine polietilena care are aplicație industrială. Un polimer este o substanță care are o greutate moleculară mare.
În interiorul macromoleculei există un anumit număr de fragmente repetate numite unități structurale. Pentru polimerizarea etilenei, gruparea - CH2—CH2- este considerată ca unitate structurală. Gradul de polimerizare indică numărul de unități repetate în structura polimerului.
Gradul de polimerizare determină proprietățile compușilor polimerici. De exemplu, polietilena cu lanț scurt este un lichid care are proprietăți lubrifiante. O macromoleculă cu lanțuri lungi se caracterizează printr-o stare solidă. Flexibilitatea și plasticitatea materialului este utilizată la fabricarea țevilor, sticlelor și foliilor. Polietilena, în care gradul de polimerizare este de cinci până la șase mii, are putere crescută, prin urmare, este utilizat în producția de fire puternice, țevi rigide și produse turnate.
Dintre produsele obținute prin polimerizarea alchenelor care au importanță practică, evidențiem clorura de polivinil. Acest compus este obținut prin polimerizarea clorurii de vinil. Produsul rezultat are caracteristici de performanță valoroase. Se caracterizează prin rezistență crescută la influențele agresive substanțe chimice, neinflamabil, ușor de vopsit. Ce se poate face din clorură de polivinil? Serviete, haine de ploaie, pânză uleioasă, piele artificială, cabluri, izolație electrică.
Teflonul este un produs al polimerizării tetrafluoretilenei. Acest compus organic inert este rezistent la schimbări bruște de temperatură.
Polistirenul este o substanță elastică transparentă formată prin polimerizarea stirenului original. Este indispensabil în fabricarea dielectricilor în inginerie radio și electrică. În plus, polistirenul este utilizat în cantități mari pentru producția de țevi rezistente la acizi, jucării, piepteni și materiale plastice poroase.
Caracteristici ale obținerii alchenelor
Reprezentanții acestei clase sunt solicitați în industria chimică modernă, astfel încât au fost dezvoltate diferite metode pentru producția lor industrială și de laborator. Etilena și omologii săi nu există în natură.
Multe opțiuni de laborator pentru obținerea reprezentanților acestei clase de hidrocarburi implică reacții de adiție inversă numite eliminare. De exemplu, dehidrogenarea parafinelor (hidrocarburi saturate) produce alchenele corespunzătoare.
Prin reacția derivaților halogenați ai alcanilor cu magneziu metalic, este posibil să se obțină și compuși cu formula generală SpH2n. Eliminarea se realizează conform regulii lui Zaitsev, inversul regulii lui Markovnikov.
În cantități industriale, hidrocarburile nesaturate din seria etilenei sunt produse prin cracarea uleiului. Gazele de cracare și piroliza petrolului și gazelor conțin de la zece până la douăzeci la sută de hidrocarburi nesaturate. Amestecul de produse de reacție conține atât parafine, cât și alchene, care sunt separate între ele prin distilare fracțională.
Unele aplicații
Alchenele sunt o clasă importantă de compuși organici. Posibilitatea utilizării lor se explică prin reactivitatea lor excelentă, ușurința în preparare și costul rezonabil. Dintre numeroasele sectoare industriale care folosesc alchene, evidențiem industria polimerilor. O cantitate imensă de etilenă, propilenă și derivații acestora este cheltuită pentru producerea de compuși polimerici.
De aceea, întrebările referitoare la căutarea unor noi modalități de producere a hidrocarburilor alchenice sunt atât de relevante.
Clorura de polivinil este considerată unul dintre cele mai importante produse obținute din alchene. Se caracterizează prin stabilitate chimică și termică și inflamabilitate scăzută. Deoarece această substanță Insolubil în solvenți minerali, dar solubil în solvenți organici, poate fi utilizat în diverse sectoare industriale.
Greutatea sa moleculară este de câteva sute de mii. Când temperatura crește, substanța este capabilă de descompunere, însoțită de eliberarea de acid clorhidric.
De un interes deosebit sunt proprietățile sale dielectrice, utilizate în ingineria electrică modernă. Dintre industriile in care se foloseste clorura de polivinil, evidentiam productia piele artificiala. Materialul rezultat caracteristici operaționaleîn nici un fel inferior material natural, având în același timp un cost mult mai mic. Îmbrăcămintea confecționată dintr-un astfel de material devine din ce în ce mai populară printre designerii de modă care creează colecții luminoase și colorate de îmbrăcăminte pentru tineret din clorură de polivinil în diferite culori.
Clorura de polivinil este folosită în cantități mari ca etanșant în frigidere. Datorită elasticității și elasticității sale, acesta component chimic la cerere în producția de filme și moderne plafoane suspendate. Tapetul lavabil este acoperit suplimentar cu o folie subțire din PVC. Acest lucru vă permite să le adăugați Putere mecanică. Astfel de Materiale de decorare va deveni varianta ideala pentru reparatii cosmeticeîn spații de birouri.
În plus, hidratarea alchenelor conduce la formarea de alcooli monohidroxilici primari și secundari, care sunt solvenți organici excelenți.
Proprietățile fizice ale alchenelor sunt similare cu cele ale alcanilor, deși toate au puțin mai mult temperaturi scăzute topindu-se și fierbinte decât alcanii corespunzători. De exemplu, pentanul are un punct de fierbere de 36 °C, iar pentena-1 - 30 °C. La conditii normale Alchenele C 2 - C 4 sunt gaze. C 5 – C 15 sunt lichide, începând de la C 16 sunt solide. Alchenele sunt insolubile în apă, dar foarte solubile în solvenți organici.
Alchenele sunt rare în natură. Deoarece alchenele sunt materii prime valoroase pentru sinteza organică industrială, au fost dezvoltate multe metode de preparare a acestora.
1. Principala sursă industrială de alchene este cracarea alcanilor care fac parte din ulei:
3. În condiții de laborator, alchenele se obțin prin reacții de eliminare, în care se elimină doi atomi sau două grupe de atomi din atomii de carbon vecini și se formează o legătură p suplimentară. Astfel de reacții includ următoarele.
1) Deshidratarea alcoolilor are loc atunci când sunt încălziți cu agenți de îndepărtare a apei, de exemplu cu acid sulfuric la temperaturi de peste 150 ° C:
Când H 2 O este eliminat din alcooli, HBr și HCl din halogenuri de alchil, atomul de hidrogen este eliminat de preferință de cel al atomilor de carbon vecini care este legat de cel mai mic număr de atomi de hidrogen (din atomul de carbon cel mai puțin hidrogenat). Acest model se numește regula lui Zaitsev.
3) Dehalogenarea are loc atunci când dihalogenurile care au atomi de halogen la atomi de carbon adiacenți sunt încălzite cu metale active:
CH2Br -CHBr -CH3 + Mg → CH2 =CH-CH3 + Mg Br2.
Proprietățile chimice ale alchenelor sunt determinate de prezența unei duble legături în moleculele lor. Densitatea electronică a legăturii p este destul de mobilă și reacționează ușor cu particulele electrofile. Prin urmare, multe reacții ale alchenelor decurg în funcție de mecanism adiție electrofilă, desemnat prin simbolul A E (din engleză, adaos electrofil). Reacțiile de adiție electrofile sunt procese ionice care au loc în mai multe etape.
În prima etapă, o particulă electrofilă (cel mai adesea acesta este un proton H +) interacționează cu electronii p ai dublei legături și formează un complex p, care este apoi transformat într-un carbocation prin formarea unei legături s covalente între particula electrofilă și unul dintre atomii de carbon:
carbocation alchenic al complexului p
În a doua etapă, carbocationul reacționează cu anionul X, formând o a doua legătură s datorită perechii de electroni a anionului:
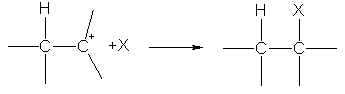
În reacțiile de adiție electrofile, un ion de hidrogen se atașează de atomul de carbon la legătura dublă care are o sarcină negativă mai mare. Distribuția sarcinii este determinată de schimbarea densității electronilor p sub influența substituenților:  .
.
Substituenții donatori de electroni care prezintă efectul +I schimbă densitatea electronului p la un atom de carbon mai hidrogenat și creează o sarcină negativă parțială asupra acestuia. Aceasta explică regula lui Markovnikov: atunci când se adaugă molecule polare precum HX (X = Hal, OH, CN, etc.) la alchenele nesimetrice, hidrogenul se atașează de preferință la atomul de carbon mai hidrogenat la legătura dublă.
Sa luam in considerare exemple concrete reacții de adiție.
1) Hidrohalogenare. Când alchenele interacționează cu halogenuri de hidrogen (HCl, HBr), se formează halogenuri de alchil:
CH3-CH = CH2 + HBr® CH3-CHBr-CH3.
Produșii de reacție sunt determinați de regula lui Markovnikov.
Cu toate acestea, trebuie subliniat că, în prezența oricărui peroxid organic, moleculele polare de HX nu reacţionează cu alchenele conform regulii lui Markovnikov:
| R-O-O-R | ||
| CH3-CH = CH2 + HBr | CH3-CH2-CH2Br |
Acest lucru se datorează faptului că prezența peroxidului determină mai degrabă mecanismul radical al reacției decât cel ionic.
2) Hidratarea. Când alchenele reacţionează cu apa în prezenţa acizilor minerali (sulfuric, fosforic), se formează alcooli. Acizii minerali acționează ca catalizatori și sunt surse de protoni. Adăugarea de apă urmează, de asemenea, regula lui Markovnikov:
CH3-CH = CH2 + HON® CH3-CH(OH)-CH3.
3) Halogenare. Alchenele decolorează apa cu brom:
CH2 = CH2 + Br2® B-CH2-CH2Br.
Această reacție este calitativă pentru o legătură dublă.
4) Hidrogenarea. Adăugarea de hidrogen are loc sub acțiunea catalizatorilor metalici:
unde R = H, CH3, CI, C6H5 etc. Molecula CH 2 =CHR se numește monomer, compusul rezultat se numește polimer, numărul n este gradul de polimerizare.
Polimerizarea diverșilor derivați de alchenă produce produse industriale valoroase: polietilenă, polipropilenă, clorură de polivinil și altele.
Pe lângă în plus, alchenele suferă și reacții de oxidare. În timpul oxidării ușoare a alchenelor cu o soluție apoasă de permanganat de potasiu (reacția Wagner), se formează alcooli dihidroxilici:
ZSN2 =CH2 + 2KMnO4 + 4H2O® ZNOSN2-CH2OH + 2MnO2↓ + 2KOH.
Ca urmare a acestei reacții, soluția violetă de permanganat de potasiu se decolorează rapid și precipită un precipitat maro de oxid de mangan (IV). Această reacție, ca și reacția de decolorare a apei cu brom, este calitativă pentru o legătură dublă. În timpul oxidării severe a alchenelor cu o soluție de fierbere de permanganat de potasiu într-un mediu acid, legătura dublă este complet ruptă cu formarea de cetone, acizi carboxilici sau CO2, de exemplu:
| [DESPRE] | ||
| CH3-CH=CH-CH3 | 2CH3-COOH |
Pe baza produșilor de oxidare, se poate determina poziția dublei legături în alchena originală.
Ca toate celelalte hidrocarburi, alchenele ard și, cu mult aer, formează dioxid de carbon și apă:
CnH2n+Zn/2O2®nCO2+nH2O.
Când aerul este limitat, arderea alchenelor poate duce la formarea de monoxid de carbon și apă:
CnH2n + n02® nCO + nH20.
Dacă amestecați o alchenă cu oxigen și treceți acest amestec peste un catalizator de argint încălzit la 200°C, se formează un oxid de alchenă (epoxialcan), de exemplu:

La orice temperatură, alchenele sunt oxidate de ozon (ozonul este un agent oxidant mai puternic decât oxigenul). Dacă ozonul gazos este trecut printr-o soluție de alchenă în tetraclorura de metan la temperaturi sub temperatura camerei, are loc o reacție de adiție și se formează ozonidele corespunzătoare (peroxizi ciclici). Ozonidele sunt foarte instabile și pot exploda ușor. Prin urmare, de obicei nu sunt izolate, dar imediat după producție sunt descompuse cu apă - aceasta produce compuși carbonilici (aldehide sau cetone), a căror structură indică structura alchenei care a fost supusă ozonării.
Alchenele inferioare sunt materii prime importante pentru sinteza organică industrială. Alcoolul etilic, polietilena și polistirenul sunt produse din etilenă. Propena este utilizată pentru sinteza polipropilenei, fenolului, acetonei și glicerinei.

