ГОССУДАРСТВЕННАЯ КОРПОРАЦИЯ
ПО АТОМНОЙ ЭНЕРГИИ «РОСАТОМ»
ФГОУ СПО «Южно-Уральский политехнический колледж»
Курсовая работа
по дисциплине: «Технология неорганических веществ»
Тема: «Двойной суперфосфат»
Выполнил:
студентка
гр. ХТ – 72 Н.И.Байрамова
Проверил: В.Н. Десятник
г. Озерск
|
Введение | ||
|
Открытие фосфора | ||
|
Фосфор в природе | ||
|
Фосфорные удобрения | ||
|
Двойной суперфосфат | ||
|
Химизм процесса | ||
|
Способы и параметры производства | ||
|
Технологические расчеты | ||
|
Список литературы |
1.Введение
Суперфосфат – смесь Ca(H 2 PO 4) 2 *H 2 O и CaSO 4 . Это наиболее распространённое минеральное фосфорное удобрение. Фосфор в суперфосфате присутствует в основном в виде монокальцийфосфата и свободной фосфорной кислоты. Удобрение содержит гипс и др. примеси (фосфаты железа и алюминия, кремнезём, соединения фтора и др.). Получают суперфосфат из природных фосфатов (апатита и фосфорита) или апатитового концентрата, обрабатывая их серной кислотой, по реакции:
Са 3 (РО 4) 2 + 2H 2 SO 4 = Сa(H 2 PO 4) 2 + 2CaSO 4 .
Для получения двойного суперфосфат апатит или фосфорит обрабатывают фосфорной кислотой.
Производят несколько видов суперфосфатов. Простой суперфосфат – серый порошок, почти не слёживаемый, среднерассеваемый; в удобрении 14-19,5% усвояемой растениями P 2 O 5 . Его получают действием H 2 SO 4 на природные фосфаты (апатиты, фосфориты). Гранулированный суперфосфат получают из простого (порошковидного), увлажняя его и окатывая в гранулы (диаметр их в основном 2-4 мм) во вращающихся барабанах. Имеет повышенную рассеваемость. Обогащенный суперфосфат получают при разложении фосфатного сырья смесью H 2 SO 4 и Н 3 РО 4 ; по составу это продукт промежуточный между простым и двойным суперфосфатами и содержит 24-32% усвояемого Р 2 О 5 . Двойной суперфосфат производят действием Н 3 РО 4 на природные фосфаты. Он содержит 45-48% усвояемой растениями P 2 O 5 , очень мало гипса, выпускается преимущественно гранулированным. В состав аммонизированного суперфосфата, кроме 14-19,5% Р 2 О 5 входит не менее 1,6% аммиака; марганизированного суперфосфата – 1,5-2,5% марганца; борного суперфосфата – 0,1-0,3% бора; молибденового суперфосфата – 0,1% молибдена.
Суперфосфат применяют на всех почвах в качестве основного предпосевного, припосевного (лучше гранулированный суперфосфат) удобрения и в подкормки. Особенно эффективен на щелочных и нейтральных почвах. В кислой почве фосфорная кислота удобрения превращается в труднодоступные растениям фосфаты алюминия и железа. В этом случае действие суперфосфата повышается при смешивании его перед внесением с фосфоритной мукой, известняком, мелом, перегноем при применении на известкованных полях. Суперфосфат ускоряет рост и цветение растений, способствует быстрому созреванию плодов и развитию корневой системы. Хранится в закрытых складских помещениях, исключающих попадание осадков и грунтовых вод.
2.Открытие фосфора.
История открытия химических элементов полна личных драм, различных неожиданностей, таинственных загадок и удивительных легенд. Успех оказывался верным спутником тех, кто умел пристально всматриваться в природные явления.
Древние фолианты сохранили для нас отдельные эпизоды из жизни отставного солдата и гамбургского купца. Звали его Хенниг Бранд (1630-?). Его купеческие дела шли не блестяще, и именно по этой причине он стремился выбраться из нищеты. Она его ужасно угнетала. И Бранд решил попытать счастья в алхимии. Тем более что в XVII веке считалось вполне возможным найти «философский камень», который способен превращать неблагородные металлы в золото.
Бранд провел уже множество опытов с различными веществами, но ничего дельного у него не получалось. Однажды он решил провести химический эксперимент с мочой. Выпарил ее почти досуха и оставшийся светло-желтый осадок смешал с углем и песком, нагревая в реторте без доступа воздуха. В результате Бранд получил новое вещество, которое обладало удивительным свойством – светиться в темноте. Так в 1669 г. был открыт фосфор, играющий исключительно важную роль в живой природе: в растительном мире, в организме животных и человека. Счастливый ученый не замедлил воспользоваться необычным свойством нового вещества и стал демонстрировать светящийся фосфор знатным особам за довольно высокое вознаграждение. Все, что соприкасалось с фосфором, приобретало способность светиться. Достаточно было помазать фосфором пальцы, волосы или предметы, и они вспыхивали таинственным голубовато-белым светом. Религиозно и мистически настроенные богатые люди того времени диву давались, смотря на различные манипуляции Бранда с этим «божественным» веществом. Он ловко использовал огромный интерес ученых и широкой публики к фосфору и стал продавать его по цене, превосходившей даже стоимость золота. X. Бранд производил фосфор в больших количествах и держал способ его получения в строжайшей тайне. Никто из других алхимиков не мог проникнуть в его лабораторию, и поэтому многие из них стали лихорадочно ставить различные опыты, стремясь раскрыть секрет изготовления фосфора.
В 1680г. секрет получения фосфора был открыт в Англии знаменитым химиком Р. Бойлем. После смерти Р. Бойля его ученик немец А. Ганквиц, улучшив методику получения фосфора, наладил его производство и даже попытался изготовить первые спички. Он снабжал фосфором научные учреждения Европы и отдельных лиц, желающих приобрести его. Для расширения торговых связей А. Ганквиц посетил Голландию, Францию, Италию и Германию, заключая новые договора на продажу фосфора. В Лондоне им была основана фармацевтическая фирма, получившая широкую известность.
Лишь столетие спустя после обнаружения фосфора он перешел из мира торговли и наживы в мир науки.
3.Фосфор в природе
Фосфор по своей важности ничуть не уступает азоту. Он участвует в великом природном круговороте веществ, и, не будь фосфора, растительный и животный мир был бы совсем иным. Однако фосфор встречается в природных условиях не так уж часто, в основном в виде минералов, и на его долю приходится 0,08% массы земной коры. По распространенности он занимает тринадцатое место среди других элементов. Интересно отметить, что в теле человека на долю фосфора приходится примерно 1,16%. Из них 0,75% уходит на костную ткань, около 0,25% – на мышечную и примерно 0,15% – на нервную ткань. Фосфор редко встречается в больших количествах, и в целом его следует отнести к рассеянным элементам. В свободном виде в природе он не обнаружен, так как обладает очень важным свойством – легко окисляется, но содержится во многих минералах, число которых уже составляет 190. Главнейшие из них - фторапатит, гидроксилапатит, фосфорит. Несколько реже встречаются вивианит, монацит, амблигонит, трифилит и совсем в ограниченных количествах - ксенотит и торбернит.
Что касается минералов фосфора, то они делятся на первичные и вторичные. Среди первичных наиболее распространены апатиты, представляющие в основном породы магматического происхождения. Химический состав апатита - фосфат кальция, содержащий некоторое количество фторида и хлорида кальция. Кроме того, они содержат от 5 до 36% Р 2 О 5 . Обычно эти минералы в большинстве случаев встречаются в зоне магмы, но нередко они обнаруживаются в местах, где изверженные породы соприкасаются с осадочными. Из всех известных месторождений фосфатов наиболее значительные имеются в Норвегии и Бразилии. Крупное отечественное месторождение апатитов открыто академиком А. Е. Ферсманом в Хибинах в 1925 г. «Апатит в основном соединение фосфорной кислоты и кальция, – писал А. Е. Ферсман. –Внешний вид этого минерала так разнообразен и странен, что старые минералоги назвали его апатитом, что значит по-гречески «обманщик». То это прозрачные кристаллики, до мелочей напоминающие берилл или даже кварц, то это плотные массы, неотличимые от простого известняка, то это радиально-лучистые шары, то порода зернистая и блестящая, как крупнозернистый мрамор».
Апатиты в результате действия процессов выветривания, жизнедеятельности бактерий, разрушения различными почвенными кислотами переходят в формы, легко потребляемые растениями, и таким образом вовлекаются в биохимический круговорот. Следует отметить, что фосфор усваивается только из растворенных солей фосфорной кислоты. Однако фосфор из почвы частично вымывается, а большое количество его, поглощенное растениями, не возвращается обратно в почву и уносится вместе с урожаем. Все это приводит к постепенному истощению почвы. При внесении в почву фосфорных удобрений урожайность увеличивается.
Несмотря на значительные потребности в фосфорных удобрениях, особых опасений, связанных с истощением запасов сырья, для их производства, по всей видимости, нет. Эти удобрения могут быть получены при комплексной переработке минерального сырья, донных морских отложений и различных геологических пород, богатых фосфором. При разложении богатых фосфором соединений органического происхождения нередко образуются газообразные и жидкие вещества. Иногда можно наблюдать выделение газа с запахом гнилой рыбы – фосфористого водорода, или фосфина, РН 3 . Одновременно с фосфином идет образование другого продукта – дифосфина, Р 2 Н 4 , представляющего собой жидкость. Пары дифосфина самовоспламеняются и поджигают газообразный фосфин.
Фосфин и дифосфин в природе встречаются довольно редко, и чаще приходится иметь дело с такими соединениями фосфора, как фосфориты. Это вторичные минералы-фосфаты органического происхождения, играют особо важную роль в сельском хозяйстве. На островах Тихого океана, в Чили и Перу они образовались на основе птичьего помета – гуано, который в условиях сухого климата накапливается мощными слоями, нередко превышающими сотню метров.
Образование фосфоритов может быть связано и с геологическими катастрофами, например с ледниковым периодом, когда гибель животных носила массовый характер. Подобные процессы возможны и в океане при массовой гибели морской фауны. Быстрое изменение гидрологических условий, которое может быть связано с различными процессами горообразования, в частности с действием подводных вулканов, несомненно, в отдельных случаях приводит к смерти морских животных. Фосфор из органических остатков частично усваивается растениями, но в основном, растворяясь в морской воде, переходит в минеральные формы. Морская вода содержит фосфаты в довольно больших количествах – 100-200 мг/м 3 . При определенных химических процессах в морской воде фосфаты могут выпадать в осадок и скапливаться на дне. А при поднятии морского дна в различные геологические периоды залежи фосфоритов оказываются на суше. Подобным образом могло образоваться крупное отечественное месторождение фосфоритов вблизи Кара-Тау в Казахстане. Встречаются фосфориты и в Подмосковье.
Рис. 1 Круговорот фосфора в природе
4.Фосфорные удобрения
Фосфорные удобрения, содержат в качестве основного питательного элемента фосфор. Различают следующие виды фосфорных удобрений:
водорастворимые – аммофос, диаммофос, суперфосфаты;
цитраторастворимые – растворимые в щелочном растворе цитрата аммония (преципитат и др.);
лимоннорастворимые - растворимые в 2%-ном водном растворе лимонной кислоты (обесфторенные фосфаты, плавленый магниевыйфосфат, термофосфаты, фосфатные сталеплавильные шлаки и др.);
труднорастворимые - очень плохо растворимые в слабых кислотах, не растворимые в воде (фосфоритная мука, костная мука).
Степень растворимости фосфорных удобрений определяет желательные размеры их частиц. Водорастворимые удобрения используют в основном в виде гранул (1-4 мм), цитрато- и лимоннорастворимые - обычно в виде порошков, труднорастворимые - только в виде тонкодисперсных порошков.
Основное сырье для производства большинства фосфорных удобрений – природные фосфаты. Способы их переработки: кислотное разложение (H 2 SO 4 или H 3 PO 4 - суперфосфаты); электровозгонка и последующее окисление фосфора с образованием термической H 3 PO 4 (двойной суперфосфат); гидротермическое разложение с удалением фтора и переводом фосфора в цитрато- и лимоннорастворимые формы (обесфторенные фосфаты); спекание или сплавление с соединениями щелочных и щелочно-земельных металлов (термофосфаты); дробление, сушка и тонкое измельчение (фосфоритная мука).
Среди всех видов фосфорных удобрений наиболее универсальны водорастворимые удобрения, которые применяют на любых почвах под все сельско-хозяйственные культуры при допосевном (основном), припосевном (напр., в рядки) и послепосевном (для подкормки) способах внесения. Цитрато- и лимоннорастворимые удобрения также используют на любых почвах под все культуры, но преимущественно для основного внесения под вспашку. Этим же способом вносят в кислые почвы в более высоких дозах труднорастворимые удобрения.
Главная продукция промышленности фосфорных удобрений – водорастворимые удобрения (90% от общей выработки).
5. Двойной суперфосфат
Двойной суперфосфат – концентрированное водорастворимое удобрение, получаемое разложением молодого природного фосфата фосфорной кислотой. По внешнему виду это гранулированный продукт серого цвета различных оттенков – от светло-серого, почти белого, до темно-серого, – содержащий некоторое количество жидкой фазы.
Основным компонентом двойного суперфосфата является моногидрат монокальцийфосфата Са(Н 2 РО 4) 2 *Н 2 О. Монокальцийфосфат – самое концентрированное водорастворимое бесхлорное фосфорно-калийное удобрение с общим содержанием питательных элементов 86%. Высокое содержание фосфора и калия обеспечивает его эффективное использование на почвах с низким уровнем плодородия.
Состав монокальцийфосфата
Двойной суперфосфат отличается небольшим содержанием других компонентов, образующихся из примесей фосфорной кислоты и природных фосфатов (сульфат кальция, фосфаты железа и алюминия, мономагний-фосфат, кремнефториды, а также непрореагировавший фосфат, дикальцийфосфат, свободная фосфорная кислота и свободная влага).
6. Химизм процесса
При разложении фосфатов фосфорной кислотой происходят следующие основные реакции:
Ca 5 (PO 4) 3 F + 7Н 3 РO 4 + 5Н 2 O = 5Са(Н 2 РО 4) 2 *Н 2 О + НF
CaCO 3 + 2H 3 PO 4 = Ca(H 2 PO 4) 2 *H 2 O + CO 2
(Ca, Mg)CO 3 + 4H 3 PO 4 = Са(Н 2 РО 4) 2 *Н 2 О + Mg(Н 2 РО 4) 2 *Н 2 О 2CO 2
Оксиды железа и алюминия образуют средние фосфаты:
(Al, Fe) 2 O 3 + 2H 3 PO 4 + H 2 O = 2(Al, Fe)PO 4 *2H 2 O
Средние фосфаты алюминия и железа обладают отрицательным температурным коэффициентом растворимости: с повышением температуры ускоряется их кристаллизация. Аморфный АlРО 4 *2H 2 О медленно превращается в комплексные соли СаАlН(Р0 4) 2 *6Н 2 O, СаАl 6 H 4 (PO 4) 8 *2H 2 O и СаАl 6 Н 4 (РО 4) 8 *2Н 2 О. Аморфный фосфат FеРO 4 *H 2 O образуется только при избытке Fе 2 О 3 в жидкой фазе. Чаще всего при достижении рН 2 реакция идет с образованием СаFе 2 Н 4 (РО 4)4*5Н 2 O.
Выделяющийся НF взаимодействует с диоксидом кремния с образованием Н 2 SiF 6 и SiF 4:
4HF + SiO 2 = SiF 4 + 2H 2 O
SiF 4 + 2HF = H 2 SiF 6
Кремнефтористоводородная кислота превращается в кремнефториды кальция, натрия и калия, а тетрафторид кремния частично выделяется в газообразном состоянии. Причем степень его выделения возрастает с повышением температуры и концентрации P 2 О 5 в жидкой фазе.
Протекание основных реакций сопровождается возрастанием температуры, а следовательно, и парциального давления паров SiF 4 . В процессе сушки при температуре более 70°С кремнефторид кальция разлагается по реакции:
СаSiF 6 (тв) + 2Н + (ж) → Н 2 SiF 6 (ж) + Са 2+ (ж) → SiF 4 (газ) + СаF 2 (тв) + 2Н + (ж)
Ион алюминия, попадающий в раствор в результате разложения побочных минералов фосфатных руд (нефелина, глауконита и глин), взаимодействует с ионами F - и SiF 6 2- с образованием более прочных комплексов [АlF] 2+ , чем аналогичные соединения кремния. Образование их задерживает выделение фтористых соединений в газовую фазу.
Норма фосфорной кислоты
Стехиометрическую норму НзРО 4 (n) на 100 массовых частей фосфорита подсчитывают по формуле:

 ,
,
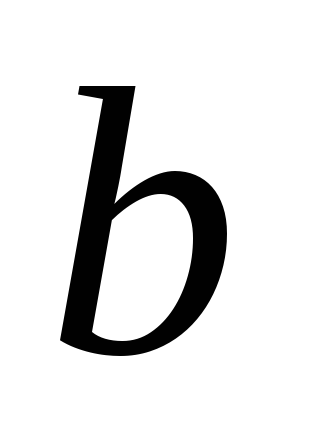 ,
, ,
, и
и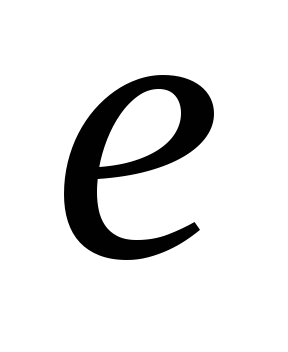 – содержание в фосфатесоответственно
СаО, МgО,
Fе 2 О 3 ,
Аl 2 О 3
и Р 2 О 5 ,
%;
– содержание в фосфатесоответственно
СаО, МgО,
Fе 2 О 3 ,
Аl 2 О 3
и Р 2 О 5 ,
%;
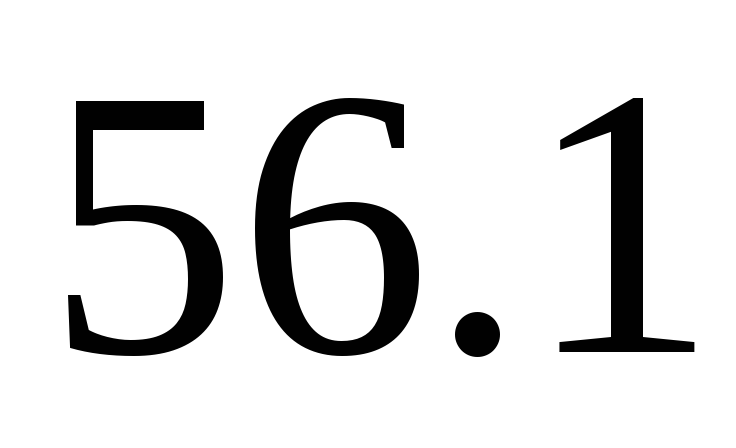 ;
;
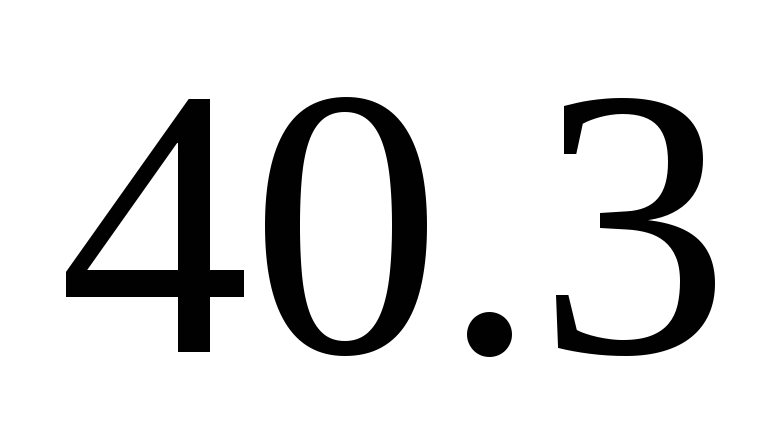 ;
; ;
;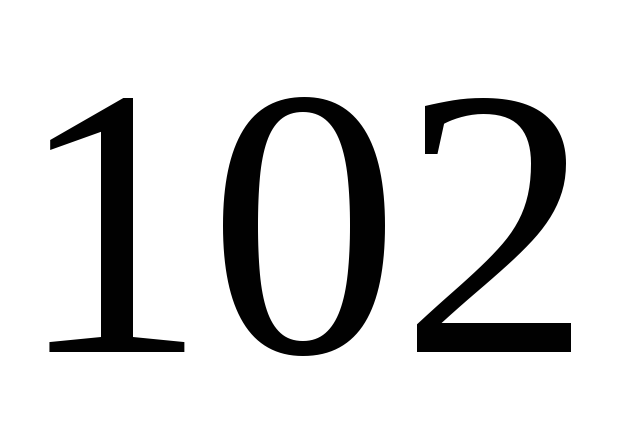 ;
;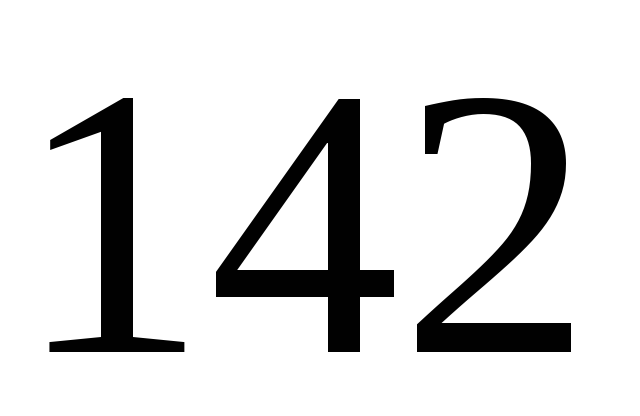 –масса
1 моль соответствующих компонентов;
–масса
1 моль соответствующих компонентов;
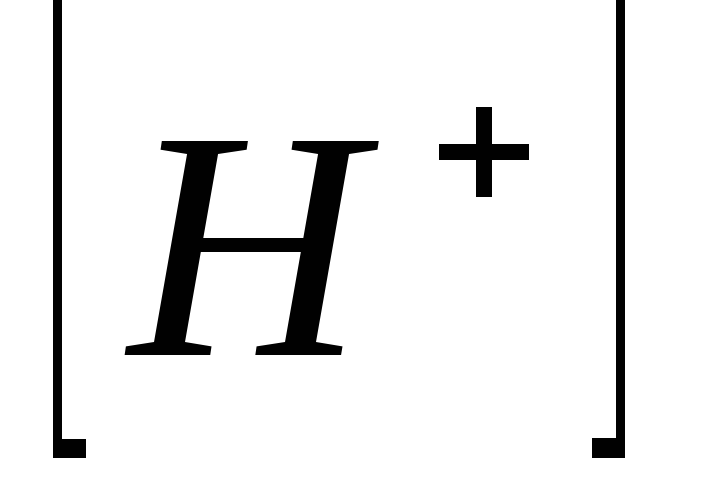 – концентрация
ионов водорода в фосфорной
кислоте.
– концентрация
ионов водорода в фосфорной
кислоте.
При разложении апатитового концентрата норму фосфорной кислоты подсчитывают по формуле:
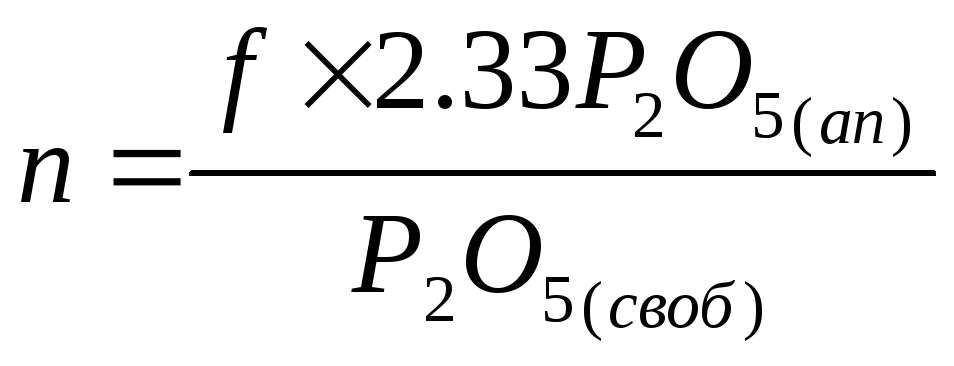
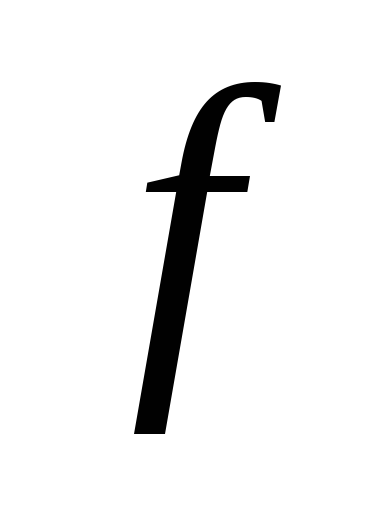 – принимаемая
доля от стехиометрической нормы;
– принимаемая
доля от стехиометрической нормы;
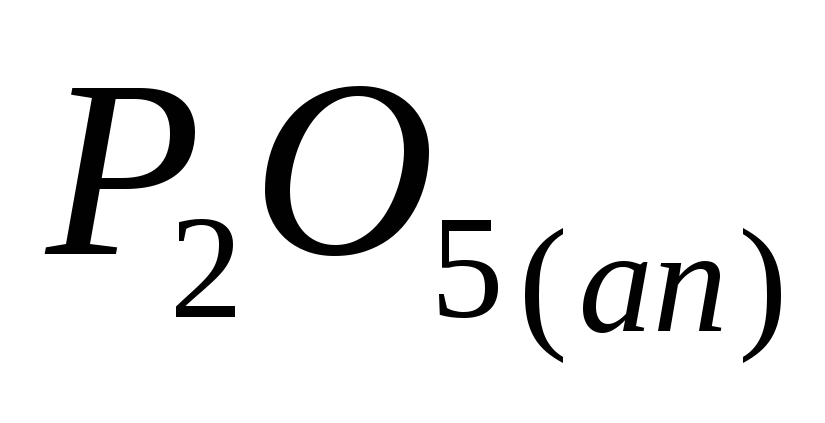 – содержание
Р 2 О 5
в апатитовом концентрате, %;
– содержание
Р 2 О 5
в апатитовом концентрате, %;
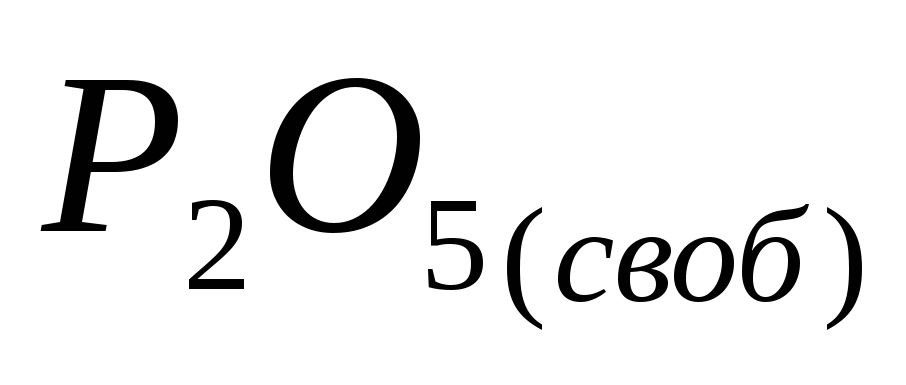 – содержание
в фосфорной кислоте свободной
Р 2 О 5 ,
%;
– содержание
в фосфорной кислоте свободной
Р 2 О 5 ,
%;
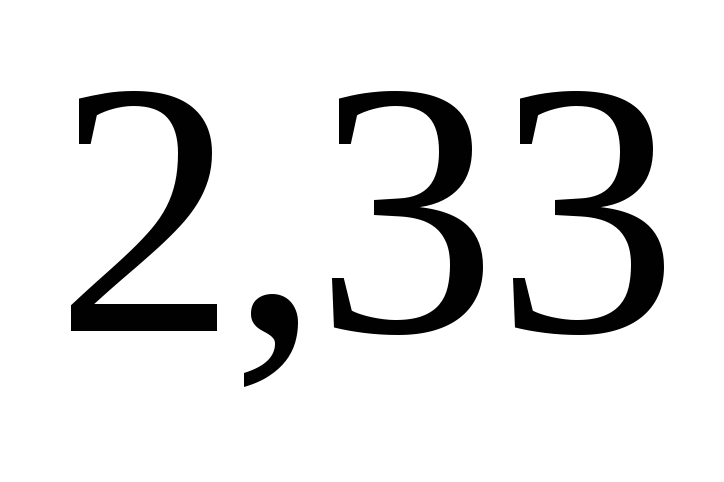 – потребность
Р 2 О 5
кислоты,
масс. ч. на 1 масс. ч. Р 5 О 5
в апатите.
– потребность
Р 2 О 5
кислоты,
масс. ч. на 1 масс. ч. Р 5 О 5
в апатите.
Добавление
к фосфорной кислоте таких
сильных кислот, как азотная, соляная,
кремнефтористоводородная и
серная, либо их смесей ускоряет
фосфорнокислотное
разложение фосфатов.
При разложении фосфата смесью
кислот следует определить суммарную
норму кислот в пересчете
на
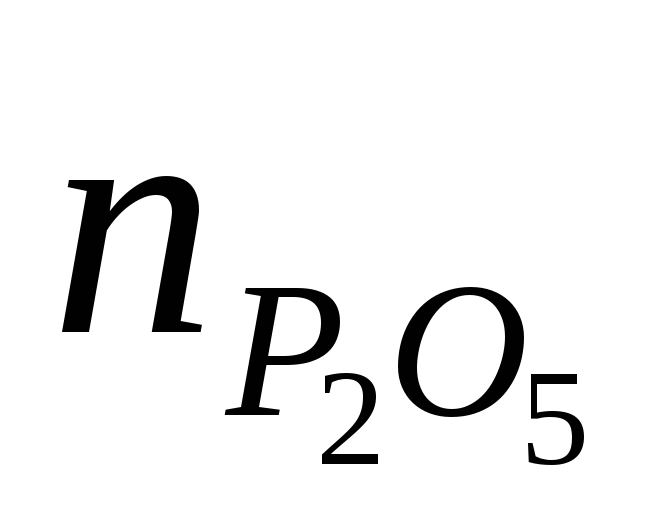 или
или
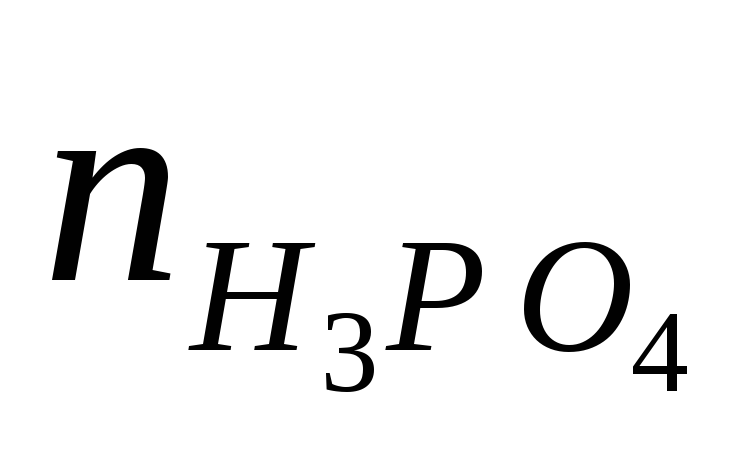 .
Разницамежду
суммарной нормой, не превышающей
стехиометрическую (в пересчете
на фосфорную кислоту), и нормой
фосфорной кислоты составляет долю
серной кислоты, выраженную в
.
Разницамежду
суммарной нормой, не превышающей
стехиометрическую (в пересчете
на фосфорную кислоту), и нормой
фосфорной кислоты составляет долю
серной кислоты, выраженную в
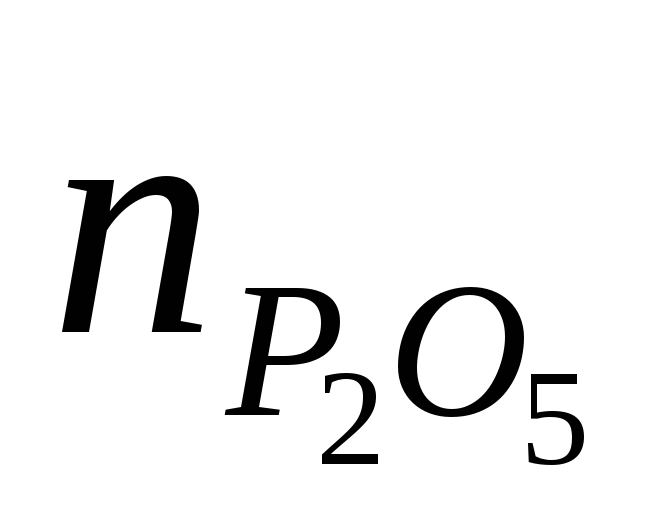 или
или
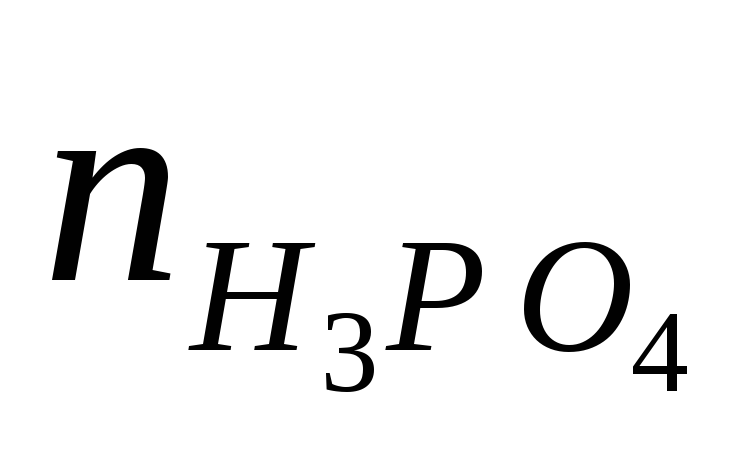 .
Для пересчета на
норму серной кислоты необходимо
учитывать,
что на разложение 1 моль апатита
расходуется 7 моль фосфорной
кислоты, а серной кислоты в два
раза меньше:
.
Для пересчета на
норму серной кислоты необходимо
учитывать,
что на разложение 1 моль апатита
расходуется 7 моль фосфорной
кислоты, а серной кислоты в два
раза меньше:
2Са 5 (РО 4) 3 F + 7Н 2 SО 4 + 6,5Н 2 О = 3Ca(H 2 PO 4) 2 *H 2 O + 7CaSO 4 *0,5H 2 O + HF
При очень большом избытке фосфорной кислоты (400-500%) можно практически нацело разложить фторапатит. Обычно берут 105-110% кислоты от стехиометрического ее количества. Увеличение нормы фосфорной кислоты сверх оптимальной незначительно повышает степень разложения фосфата, но значительно ухудшает физические свойства двойного суперфосфата и увеличивает содержание в нем свободной кислотности.
Условия равновесия и кристал лизация твердых фаз
Знание этих условий весьма важно для правильного выбора технологического режима.
Процесс разложения фосфатов фосфорной кислотой состоит из двух стадий – растворения фосфата в растворах фосфорной кислоты, вначале ненасыщенных, а затем насыщенных фосфатами кальция. Эти стадии различаются по своим равновесным, а также кинетическим условиям.
Наибольшее разложение апатита в равновесных условиях достигается при более низких температурах и концентрациях фосфорной кислоты. Степень разложения фосфата в момент насыщения жидкой фазы составляет 5-7%.
Дальнейшее разложение фосфата во II стадии происходит при взаимодействии его с насыщенным раствором и сопровождается выделением твердой фазы. Данные о равновесии в системе могут быть использованы для выбора условий кристаллизации твердой фазы того или иного состава. При образовании в I стадии насыщенных эвтонических растворов, дальнейшее разложение сопряжено с выделением в твердую фазу вначале смеси моно- и дикальцийфосфата, а к концу процесса – одного дикальцийфосфата.
Кинетика разложения фосфатов
В производстве двойного суперфосфата растворение природного фосфата в Н 3 РО 4 (5-10 мин) сопровождается образованием частично нейтрализованного раствора фосфорной кислоты (I стадия), а затем, после его насыщения, в течение длительного времени – образованием также твердой фазы (II стадия).
Оптимальный режим разложения фосфата может быть установлен с учетом равновесных и кинетических условий на каждой стадии процесса.
Разложение фосфата фосфорной кислотой
Скорость разложения фосфата фосфорной кислотой (без кристаллизации твердой фазы) с образованием гомогенного раствора определяется законами диффузионных процессов. По мере нейтрализации свободной кислоты и ионов кальция вплоть до образования насыщенного раствора скорость процесса уменьшается.
При значительном избытке кислоты по отношению к реагирующему фосфату и абсолютно малой степени нейтрализации кислоты скорость разложения фосфата достаточно велика даже при использовании кислоты относительно небольшой концентрации.
Наибольшая скорость растворения апатита достигается при следующих концентрациях растворов, равновесных с Са(Н 2 РО 4) 2 *Н 2 О:
По мере приближения состава жидкой фазы к составу насыщенного раствора существенное значение приобретает концентрация водородных ионов среды. Скорость разложения фосфорита в насыщенных СаНРО 4 растворах очень мала вследствие низкой активности водородных ионов в этих условиях. В растворах, насыщенных Са(Н 2 РО 4) 2 , активность ионов Н + резко возрастает, повышается и скорость разложения.
С повышением температуры увеличивается скорость взаимодействия водородных ионов с апатитом. Одновременно снижается концентрация ионов водорода в растворе. Суммарное действие двух противоположных эффектов, вызываемых повышением температуры, приводит к практической независимости скорости разложения апатита в тройной системе СаО – Р 2 О 5 – Н 2 О от температуры.
Суперфосфат двойной – является азотно-фосфорным, концентрированным удобрением, которое подходит для применения на любых почвах под разнообразные культуры. Для того, чтоб получить двойной суперфосфат, фосфорит обрабатывают фосфорной кислотой, которую получили из апатита, серной кислоты и фосфорита.
Удобрение можно вносить любым способом: как основное, предпосевное средство и непосредственно в почву при посеве.
Химические свойства:
Суперфосфат двойной формула: Са(Н 2 РО 4) 2 х Н 2 О.
Химический состав: фосфор (Р) – 43-46%; азот (N) — 10%; сера(S) — 5%, а также содержатся микроэлементы: цинк, медь, железо, бор, молибден, марганец.
Особенности применения:
- Благодаря присутствию в составе серы, растения проявляют более жизнестойкость, у масличных культур существенно повышается содержание жирности в семенах, у зерновых культур – количество содержащегося белка.
- Способствует повышению урожая, а также качества продукции.
- Ускоряет процесс созревания урожая.
- При основном внесении, перед засевом планируемой сельскохозяйственной культуры, вносят удобрение на глубину засева семян. Такая глубина оптимальна, так как гранулы суперфосфата не смываются потоками дождя, не переходят в нижние слои грунта от первоначального внесения.
- При разбрасывании суперфосфата по поверхности почвы, эффективность существенно понижается, поскольку для питания растений, вещество, должно быть, расположено максимально близко от корневой системы.
- Для усиления действия, удобрение суперфосфат двойной используют совместно с калийными подкормками (весной), и азотно-калийными (осенью).
- При определении дозировки удобрения, следует учитывать не только тип почвы, но и свойства возделываемых культур. Например, подсолнечник и кукуруза испытывают угнетенность при прямом контакте посадочных семян с суперфосфатом. В случае применения, следует минимизировать контакт семян и минерала, выдерживая большую прослойку земли между ними, а также в таком случае следует снизить дозу удобрения.
- Удобрение не токсично, взрыво- и пожаробезопасное, не слеживается.
- В сравнении с аммофосом, суперфосфат двойной обладает лучшей растворимостью фосфора.
Уважаемые посетители, сохраните эту статью в социальных сетях. Мы публикуем очень полезные статьи, которые помогут Вам в вашем деле. Поделитесь! Жмите!
Средние нормы:
- Под ярые зерновые культуры — 100-170 кг/га;
- Для кукурузы — 120-170 кг/га;
- При посадке озимых зерновых - 120-130 кг/га;
- При проведении осенней и весенней перекопки 200-300 кг/га;
- Картофель (вносят при посадке) - 3 г/ лунка;
- При высадке рассады - 3 г/ лунка;
- Для внесения под плодовые деревья, удобряют приствольные круги по 25-30 г;
И немного о секретах...
Вы когда-нибудь испытывали невыносимые боли в суставах? И Вы не понаслышке знаете, что такое:
- невозможность легко и комфортно передвигаться;
- дискомфорт при подъемах и спусках по лестнице;
- неприятный хруст, щелканье не по собственному желанию;
- боль во время или после физических упражнений;
- воспаление в области суставов и припухлости;
- беспричинные и порой невыносимые ноющие боли в суставах...
А теперь ответьте на вопрос: вас это устраивает? Разве такую боль можно терпеть? А сколько денег вы уже "слили" на неэффективное лечение? Правильно - пора с этим кончать! Согласны? Именно поэтому мы решили опубликовать эксклюзивное интервью с профессором Дикулем , в котором он раскрыл секреты избавления от болей в суставах, артритов и артрозов.
Суперфосфат – это минеральное удобрение, для получения которого применяется метод разложения природных фосфатов. Главным составляющим данного продукта остается фосфор. Этот макроэлемент незаменим для нормального роста и формирования различных агротехнических культур. Благодаря ему удается простимулировать рост растения, повысить плодоношение, повлиять на вкусовые качества, затормозить процессы старения.
Использование двойного состава
Этот вид удобрения внедряют в грунт рано весной перед тем, как будет осуществлена посадка культуры. Также можно вводить осенью, после сбора урожая. Между внедрениями основного удобрения необходимо поливать растения 2 раза.
Задействуют двойной суперфосфат согласно следующей инструкции:
- Для достижения равномерного внедрения удобрения стоит выполнять это при помощи зерновой сеялки. Она представлена в виде гранул.
- Выполнять основное внесение двойного суперфосфата стоит до засева огородных растений. Как правило, это делают под плужок. После внесения суперфосфата гранулированное удобрение не смывается поливочными и дождевыми водами.
- Если использовать метод ручного разброса, то удастся получить более заметный результат, так как удобрение должно быть расположено максимально близко к корневой системе растения.
- Задействовать двойной суперфосфат можно в комбинации с азотно-калийными и калийными составами. Их внедряют в грунт весной и осенью.
Для удобрения всего участка, то на 1 м2 необходимо использовать 20 г суперфосфата. Данная дозировка считается стандартной для многих овощных культур.
Для помидор
 Суперфосфат активно используют для подкормки томатов. Для одного кустика буде достаточно 20 г удобрения. Глубоко располагать питательные компоненты не рекомендуется, иначе вы не добьетесь необходимого эффекта. Для достижения максимального эффекта необходимо равномерно расположить подкормку под рыхлым слоем почвы. Около 95% фосфора томаты применяют для формирования плодов. По этой причине использовать суперфосфат стоит не только весной. Целесообразно внедрять питание на момент цветения овощной культуры.
Суперфосфат активно используют для подкормки томатов. Для одного кустика буде достаточно 20 г удобрения. Глубоко располагать питательные компоненты не рекомендуется, иначе вы не добьетесь необходимого эффекта. Для достижения максимального эффекта необходимо равномерно расположить подкормку под рыхлым слоем почвы. Около 95% фосфора томаты применяют для формирования плодов. По этой причине использовать суперфосфат стоит не только весной. Целесообразно внедрять питание на момент цветения овощной культуры.
Когда в составе суперфосфата калий содержится в большом количестве, то это идеальное питание для помидор. Именно этот компонент так «любит» данный продукт. В результате такого ухода помидоры становятся более сладкими.
Как избавиться и что такое указано в статье.
У взрослых овощных культур, которые обладают отлично развитой корневой системой, процесс усваивания удобрения происходит намного быстрее. Молодые же растения хуже потребляют фосфор. Для экономии средств на момент высадки рассады в почву необходимо использовать удобрение в виде гранул. Именно такое питание культура принимает лучше всего. Для взрослых культур вполне может подойти и простой вариант данного удобрения.
Цена
Для тех, кто желает приобрести данный вид удобрения, необходимо будет отдать за 1 кг 50 – 150 рублей.
Суперфосфат – это универсальный тип удобрения, в роли главного компонента в котором выступает фосфор.
Е указана процедура посадка картофеля минитрактором окучниками.
Применять его можно на любой почве и для любых культурных растений. Такое питание приведет к тому, что растение начнет быстрее давать плоды, его корневая система станет мощнее, а вкус созревших плодов улучшится.

